? ? ? ?
? ? ? ?[摘要]:研究炸藥熱分解機理隨研究炸藥的化學(xué)穩定性����、熱爆炸等有重要的意義��。本次用ARC測試結果和測試曲線(xiàn)����,得到了絕熱分解特性參數��,并作了簡(jiǎn)單對比分析�。乳化炸藥的典型組分對乳化炸藥和硝酸銨的熱分解的影響���,具有很大的相似性;?連續相和油相組分對硝酸銨的影響顯著(zhù)�,而對乳化炸藥的影響有所下降����,乳化劑對乳化炸藥的影響則表現明顯等��。?
[關(guān)鍵詞]:??炸藥熱分解????ARC測試?
工業(yè)炸藥從制備后到使用時(shí)需要經(jīng)歷一定的儲存時(shí)間�,在這段儲存期內如何保證炸藥的穩定性��,這涉及到炸藥的安定性問(wèn)題��。炸藥的安定性是指在一定的條件下�,保持其物理����、化學(xué)和爆炸性質(zhì)不發(fā)生明顯變化的能力�。一般分為物理安定性和化學(xué)安定性���。物理安定性是指在一定的條件下���,炸藥保持其物理性質(zhì)不發(fā)生明顯變化的能力�?���;瘜W(xué)安定性是炸藥保持其化學(xué)性質(zhì)不發(fā)生明顯變化的能力��。?
炸藥的化學(xué)安定性主要是指炸藥的熱安定性�����,炸藥在貯存條件下的化學(xué)變化�,就是炸藥自身的熱分解���,也就是炸藥熱分解的性質(zhì)和速度���。炸藥的熱分解�,是指在炸藥的發(fā)火溫度下�,由于熱作用�����,其分子發(fā)生分解的現象和過(guò)程����。研究炸藥熱分解機理隨研究炸藥的化學(xué)穩定性��、熱爆炸等有重要的意義�。?
就凝聚炸藥而言�,熱分解動(dòng)力學(xué)過(guò)程可分為以下三個(gè)階段:?
1)分解初期:分解很緩慢�����,幾乎覺(jué)察不出反應的存在�,生成的氣態(tài)產(chǎn)物也很少����,這個(gè)階段稱(chēng)為分解延滯期或感應期;?
2)分解加速期:延滯期結束后��,分解速度逐漸加快�,在某一時(shí)刻速度可達到zui大值��,這個(gè)結算稱(chēng)為加速期:?
3)降速期:當炸藥量較少時(shí)����,反應速度達到zui大值后急劇下降�,直到分解結束�����,這個(gè)階段稱(chēng)為降速期���。?
但是當炸藥量較多時(shí)�����,反應速度也可能一直增長(cháng)直至爆炸�����。上述階段的劃分是按照動(dòng)力學(xué)曲線(xiàn)的性質(zhì)劃分的�,沒(méi)有涉及炸藥熱分解的微觀(guān)機理����。炸藥分子在分解時(shí)�����,并不是立即形成zui終產(chǎn)物��,而是分部分段進(jìn)行的����。?
在一般化學(xué)反應過(guò)程中�����,隨著(zhù)原始物質(zhì)濃度下降����,反應速度程下降趨勢��,但是炸藥熱分解是個(gè)放熱過(guò)程���,盡管原始物質(zhì)不斷減少�,反應速度隨著(zhù)分解溫度的升高而加速��。?
動(dòng)力學(xué)實(shí)驗結果表明���,大多數炸藥熱分解的初始反應速度常數只受溫度的影響��,它與溫度的關(guān)系可用Arrhenius方程表示:(1-1)式
式中:k為一定溫度下��,初始反應速度常數(1s?);A為指前因子;T為溫度;R為普適氣體常量(11kJKmol????)?;?E為分解反應的活化能(1kJmol??)�。?
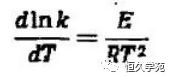
對(1-2)式可見(jiàn)��,lnk隨溫度的變化率與E值成正比����?�;罨鼙?/span>示炸藥熱分解的難易程度����,炸藥熱分解的活化能高�,熱分解反應速度的溫度系數增大�����。?
在熱分析方法中���,Le-Chatelier于1887年首先提出差熱分析(Quantitative?Differential?Thermal?Analysis,簡(jiǎn)稱(chēng)DTA)���。直到20世紀SO年代中期���,差熱分析才被應用于炸藥的熱安定性研究中���。目前�����,許多國家已將它作為篩選混合炸藥配方的標準方法��。類(lèi)似于差熱分析的差示掃描量熱儀(Differential?Scanning?Calorimetry�����,簡(jiǎn)稱(chēng)DSC)于1964年首先由Watson研制出來(lái)�,該方法的試樣用量少�,靈敏度高���,可直接測定熱焓變化����,從而使定性的差熱分析發(fā)展到定量差熱分析��。放出氣體分析法始于20世紀初��,Farmer于1920年提出真空安定性實(shí)驗方法(Vacuum?Stability?Testing�����,簡(jiǎn)稱(chēng)VST)�����,英美等國家將該法相繼作為篩選混合炸藥配方的標準方法��,雖然該方法的原理��、儀器操作都非常簡(jiǎn)單��,且作為“標準”的理論依據不是很充分�,但大量的實(shí)驗數據證明了這種方法的可靠性�����。20世紀20年代初期�����,鐮式玻璃薄膜壓力計方法在前蘇聯(lián)首先應用于炸藥的熱分解研究中����。著(zhù)名的前蘇聯(lián)科學(xué)家K.K.Andreev應用此法研究了大量的炸藥熱分解規律和熱解反應動(dòng)力學(xué)�,并在此領(lǐng)域做出了卓越的貢獻����。?
熱重(Thermal?Gravimetry����,簡(jiǎn)稱(chēng)TG)是測定物質(zhì)質(zhì)量隨溫度變化的方法���,1915年首先由日本東京大學(xué)本多光太郎發(fā)表論文��,設計了第一臺簡(jiǎn)易熱天平�。由于測定的時(shí)間較長(cháng)����,且儀器的穩定性受到限制����,熱天平?jīng)]有得到普遍應用��。而后隨著(zhù)熱分析技術(shù)的不斷完善����。上述量氣方法和熱失重方法只能直接或間接地測出釋放的氣體和揮發(fā)的總量�����,以及研究其唯象反應動(dòng)力學(xué)�,但是不能定性和定量地測出氣體中組分以及含量����,也不能闡明反應進(jìn)行的機理��。在氣相色譜法基礎上發(fā)展起來(lái)的化學(xué)反應性實(shí)驗方法(?Chemical?Reactivity?Test�,簡(jiǎn)稱(chēng)CRT)�����,于20世紀60年代初期在美國Pantex工廠(chǎng)首先被用來(lái)取代真空安定性實(shí)驗方法.這種方法不但可以準確地測定釋放氣體的總量���,而且能快速地測定NO2,CO2, H2O,CO,NO等組分的含量�����。?
?
20世紀70年代初發(fā)展起來(lái)的化學(xué)發(fā)光法��,主要用來(lái)測定在較低溫度下炸藥發(fā)生熱分解反應生成NOx的含量��,其靈敏度可達到ppb級����。這對于測定貯存溫度下炸藥的熱安定性和相容性��、預測貯存壽命具有重要的意義�����。?
熱分析技術(shù)中“控制轉化率熱分析”(?Controlled?Transformation?Rate?Thermal?Analysis�,簡(jiǎn)稱(chēng)CRTA)�。它是通過(guò)控制反應過(guò)程中氣體的溢出速率(一般保持常數)為不是通過(guò)控制溫升速率來(lái)控制反應速率����。因此適合有氣體生成的固體的分解反應�����。CRTA法有很多優(yōu)點(diǎn)��,與傳統的TA法比較��,它不必考慮升溫速率是否是常數�,在確定相互交疊的反應步驟和合適的反應機理函數,f(a)時(shí)很有效����。此外還可以明顯降低傳熱傳質(zhì)的影響�。?
溫度調制技術(shù)(Temperature?Modulation)被引入到熱分析中���,產(chǎn)生了如MDSC���,TMTG這樣的熱分析技術(shù)�。它們在熱分析過(guò)程中也發(fā)揮了重要的作用�。另外����,Paulik等人開(kāi)發(fā)的準定溫和準等壓TA技術(shù)都是很有前途的熱分析方法���。
其他熱分析方法有熱膨脹(TD)�、熱應力測定����、環(huán)境試驗和熱機械分析(TMA)等�����,以及在這些基礎上發(fā)展起來(lái)的TG-DTA,?TG-DSC,?TG-GC,?TG-DTA-GC,TG-GC-MS,?TG-GC-FTIR等連用技術(shù)����,其優(yōu)越性己經(jīng)越來(lái)越為人們所認識��。?
近年來(lái)發(fā)展起來(lái)的加速量熱儀(Accelerating?Rate?Calorimetry�����,簡(jiǎn)稱(chēng)ARC?)試驗�,是一種評價(jià)放熱性化學(xué)物質(zhì)危險性的新方法�,該方法的介紹見(jiàn)2.1�。加速量熱儀后被聯(lián)合國推薦使用的用于危險品評估的新型熱分析儀器���。通過(guò)ARC測試可得到有關(guān)放熱反應的熱力學(xué)和動(dòng)力學(xué)信息�。加速量熱儀可保證樣品在試驗環(huán)境為完全絕熱的條件下測量樣品熱分解反應過(guò)程中時(shí)間-溫度-壓力三者的變化關(guān)系���。通過(guò)建立數學(xué)模型�,可確定出放熱反應的各種動(dòng)力學(xué)參數�����。根據這些參數可以對反應對象的危險性進(jìn)行精確的預測���,較之DSC等方法有無(wú)法比擬的優(yōu)點(diǎn)�����,尤其是能給出DTA和DSC等無(wú)法給出的物質(zhì)在熱分解初期的壓力緩慢變化過(guò)程���。?
加速量熱儀是一種基于絕熱原理設計的量熱儀器�����,可使用較大的樣品量�����,靈敏度高���,能提供絕熱條件下化學(xué)反應的時(shí)間-溫度-壓力數據�����,精確測得樣品熱分解初始溫度���、絕熱分解過(guò)程中溫度和壓力隨時(shí)間的變化曲線(xiàn)�����,通過(guò)建立數學(xué)模型��,可確定出放熱反應的各種熱力學(xué)和動(dòng)力學(xué)參數���。根據這些參數可以對反應對象的危險性進(jìn)行精確的預測���。?
首先在A(yíng)RC控制器上設定起始溫度�、斜率敏感度��、加熱幅度����、終止溫度和等待時(shí)間等運行參數�����,啟動(dòng)加速量熱儀��。加速量熱儀很快將溫度升高到起始溫度���,然后按“加熱-等待-搜尋”的方式自動(dòng)操作(見(jiàn)圖2.1)�。在“加熱”階段����,加速量熱儀的溫度按設定的加熱幅度升高;在“等待”階段����,加速量熱儀建立起絕熱爐內的溫度平衡;而ARC進(jìn)入“搜尋”階段��,將試樣的溫升速率與設定的斜率敏感度相比較��,如果前者小于后者�,則自動(dòng)進(jìn)入下一個(gè)“加熱-等待-搜尋”循環(huán);如果前者大于后者�����,則加速量熱儀自動(dòng)轉為“放熱”方式���,并記錄整個(gè)反應過(guò)程中的溫度��、壓力和溫升速率等信息�����。?
2.3加速量熱儀的結構?
美國格倫比亞科學(xué)工業(yè)公司生產(chǎn)的CSI-ARC的核心部分結構如圖2.2所示�,圖中所示的球形樣品室(內徑10mm)能夠容納lOg的固體或液體樣品�����。量熱儀的殼體是用鎳銅合金制成的�����,里面安臵有三個(gè)測溫熱電偶和八個(gè)加熱器����。它們可以使殼體和樣品之間的溫度差在整個(gè)運行過(guò)程中保持很小的值�����。第四個(gè)熱電偶安臵在樣品室的外壁上�,用于探測樣品的溫度�,樣品室通過(guò)一個(gè)細管與能夠連續測量壓力變化的膜片式壓力傳感器直接相連����。?
2.4動(dòng)力學(xué)參數計算與修正?
在絕熱條件下����,加速量熱儀的絕熱溫升速率的一般方程(*)為?
其中mt,?dT/dt為反應物在溫度T時(shí)的溫升速率;?ΔTab為反應物的絕熱溫升�,ΔTab=Tf-To,號為反應結束時(shí)的溫度�����,To為反的初始放熱溫度;f(a)司為反應機理函數���,其為
通過(guò)ARC系統計算可以得到反應表觀(guān)活化能Ea��、指前因子A����、反應級數等動(dòng)力學(xué)數據���。然而方程(*)是基于這樣一種理想情況進(jìn)行的��,即認為化學(xué)反應放出的熱量只用來(lái)加熱試樣本身��,而沒(méi)有考慮反應容器的存在���。事實(shí)上����,不管是在實(shí)際應用中����,還是在A(yíng)RC測試中�����,反應放出的熱量都有一部分用來(lái)加熱反應容器��。故需要加以修正����。引入試樣容器的修正系數:??
上式中Ms為試樣量;Cvs����,為平均比熱容;為Mb試樣容器的質(zhì)量;為Cvb試樣容器的平均比熱容�。?下表列出各個(gè)參數的修正方程

? +
+
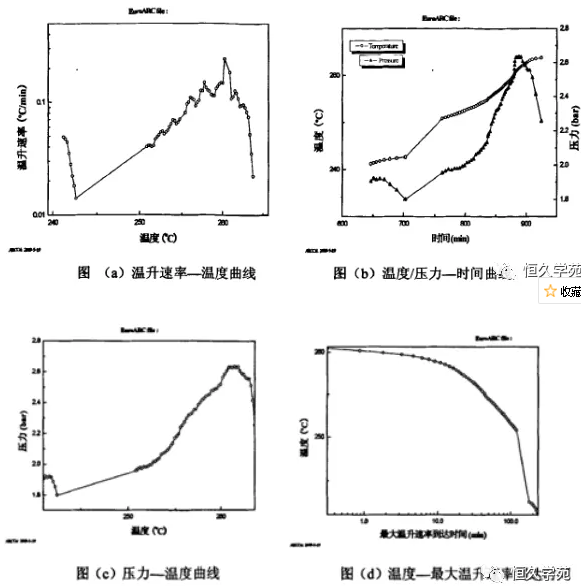
試樣測試結果如圖3.1所示�����。測試起始溫度為100℃�����,經(jīng)過(guò)19個(gè)“加熱-等待-搜尋”循環(huán)過(guò)程以后���,在241.18℃時(shí)量熱儀探測到了放熱�����,此時(shí)溫升速率為0.049℃min-1?(大于系統設定的斜率敏感度0.020℃min-1)�,隨后溫升速率持續下降����,從圖3.1?(a)中可以看到����,在242.54~250.83℃時(shí)��,出現間斷如同硝酸錢(qián)分解的間斷(兩次間斷范圍為241.07~255.81℃)�����,與SP-80/硝酸按混合體系的分解曲線(xiàn)相類(lèi)似��。之后��,在經(jīng)歷2次“加熱-等待-搜索”過(guò)程后�����,儀器重新開(kāi)始記錄數據;這說(shuō)明1#試樣在分解過(guò)程中同時(shí)伴有吸熱過(guò)程�����。從250.83℃開(kāi)始���,溫升速率緩慢增加�。235.65?min后���,在260.66℃處出現最大溫升速率0.662℃min-1��,之后溫升速率逐漸降低���。反應系統的最高分解溫度為263.75℃�����,最高分解壓力為265.321cPa��,最大壓升速率為6.851kPamin-1?
本次分別給出了它們各自的ARC測試結果和測試曲線(xiàn)�,得到了絕熱分解特性參數�,并作了簡(jiǎn)單對比分析���。?
1)與研究結果相比較���,乳化炸藥的典型組分對乳化炸藥和硝酸銨的熱分解的影響��,具有很大的相似性����,即促進(jìn)硝酸銨分解的物質(zhì)�,對乳化炸藥的熱穩定性不利�。尤其是在溫升速率和壓力變化方面���,兩者所表現出來(lái)的規律具有一致性:由于乳化炸藥體系更加復雜����,分解曲線(xiàn)也變得較為復雜;???
2)在起始分解溫度��、最高分解溫度和絕熱溫升方面�����,各組分對乳
化炸藥和硝酸銨的影響程度有所不同����。連續相和油相組分對硝酸銨的影響顯著(zhù)�,而對乳化炸藥的影響有所下降�,乳化劑對乳化炸藥的影響則表現明顯;?
3)當煤礦許用乳化炸藥組分改用上述物質(zhì)時(shí)�,其熱穩定性下降���,分解加速���。?
[1]安得列也夫著(zhù)���,石秀發(fā)譯��,炸藥的熱分解.北京:國防工業(yè)出版社?
[2]賴(lài)應得.含水工業(yè)炸藥的使用前景以及發(fā)展對策.中國煤炭�����,1999??
[3]李建軍��,王光旭.乳化炸藥熱點(diǎn)火的實(shí)驗研究.工程爆破����,1997.6??
[4]周新利���,劉祖亮���,呂春緒.巖石乳化炸藥熱分解安全性的加速量熱法分析.報����,2003.5,?26?(2):62~65?
[5]陳建平���,王瑾等�,乳化炸藥化學(xué)反應動(dòng)力學(xué)參數計算.煤���,2000.4??
[6]王光龍����,許秀成.硝酸錢(qián)熱穩定性的研究.鄭州大學(xué)學(xué)報��,2003,?24??
[7]陸明.工業(yè)炸藥配方設計.北京:北京理工大學(xué)出版社�,2002?
[8]化肥工業(yè)大全編輯委員會(huì ).化肥工業(yè)大全����。北京:化學(xué)工業(yè)出版社??